CHON: Los elementos de la química orgánica (primera parte)

F. Alejandro Sánchez Flores
Instituto de Biotecnología, UNAM. Miembro de la Academia de Ciencias de Morelos
Recordando que este año celebramos el año de la tabla periódica y su 150 aniversario, no está de más hablar de los elementos que conforman la mayoría de los compuestos que formar parte de los seres vivos. La química orgánica es la rama de la química que centra su estudio en las sustancias que contienen carbono. Es por esto que también se le conoce como la química del carbono y se encarga de conocer las propiedades, estructura, comportamiento y origen de los compuestos químicos que contienen carbono y que son fundamentales para la vida.
A diferencia de la química inorgánica que tuvo un desarrollo importante entre 1600 y 1800, no fue sino hasta el siglo XX que se comenzaron los estudios de las sustancias que provenían de las plantas y los animales. En 1828, el químico alemán Friederich Wöhler se percató que el cianato de amonio (compuesto inorgánico), podía convertirse en urea, el cual es un compuesto orgánico que podemos encontrar en la orina. Cabe mencionar que la diferencia entre un compuesto considerado orgánico y uno inorgánico, es que los orgánicos contienen siempre átomos de carbono formando enlaces covalentes con átomos de hidrogeno u otros elementos, como oxígeno, nitrógeno, azufre o fosforo.
En cambio, los compuestos inorgánicos se forman entre metales y no metales, formando enlaces iónicos o metálicos como sucede en un compuesto muy común como lo es la sal de mesa o cloruro de sodio (NaCl). Sin entrar en mucho detalle, en un enlace iónico, un elemento da su electrón de valencia al otro elemento en un comportamiento de iones de carga opuesta donde surge una atracción. Los compuestos iónicos forman redes cristalinas constituidas por una cantidad determinada de iones de carga opuesta, unidos por fuerzas electrostáticas. Si la atracción electrostática es fuerte, se forman sólidos cristalinos de elevado punto de fusión e insolubles en agua; si la atracción es menor, como en el caso del NaCl, el punto de fusión también es menor y, en general, son solubles en agua e insolubles en líquidos apolares.
Retomando el tema de los compuestos orgánicos, en esta entrega, hablaremos del primero de los cuatro elementos mas comunes encontrados en ellos que se mencionan desde el título: Carbono, Hidrogeno, Oxigeno y Nitrógeno (CHON).
El protagonista de la química orgánica: El carbono
El nombre de este elemento no metal, proviene del latín carbo que significa carbón. Podemos encontrarlo en la tabla periódica en la segunda fila en el bloque del lado extremo derecho, con el símbolo C, numero atómico 6 y masa atómica de 12.01. El carbono no se creó durante el Big Bang porque hubiera necesitado la triple colisión de partículas alfa (núcleos atómicos de helio) y el Universo se expandió y enfrió demasiado rápido para que la probabilidad de que ello aconteciera fuera significativa (http://www.acmor.org.mx/?q=content/el-origen-de-los-%C3%A1tomos). Donde sí ocurre este proceso es en el interior de las estrellas, donde este elemento es abundante y se encuentra además en otros cuerpos celestes como los cometas y en las atmósferas de otros planetas. Algunos meteoritos contienen diamantes microscópicos que se formaron cuando el Sistema Solar era aún un disco protoplanetario. En nuestro planeta, podemos encontrarlo en la corteza terrestre como una roca sedimentaria de color negro el cual conocemos como carbón mineral. De hecho, en esta forma ya se encuentra mezclado con otros elementos como azufre, nitrógeno, oxígeno, hidrógeno y nitrógeno. Esto es debido a que estas rocas en realidad eran compuestos orgánicos que se fueron acumulando a partir de materia vegetal, que existieron hace unos 300 millones de años.
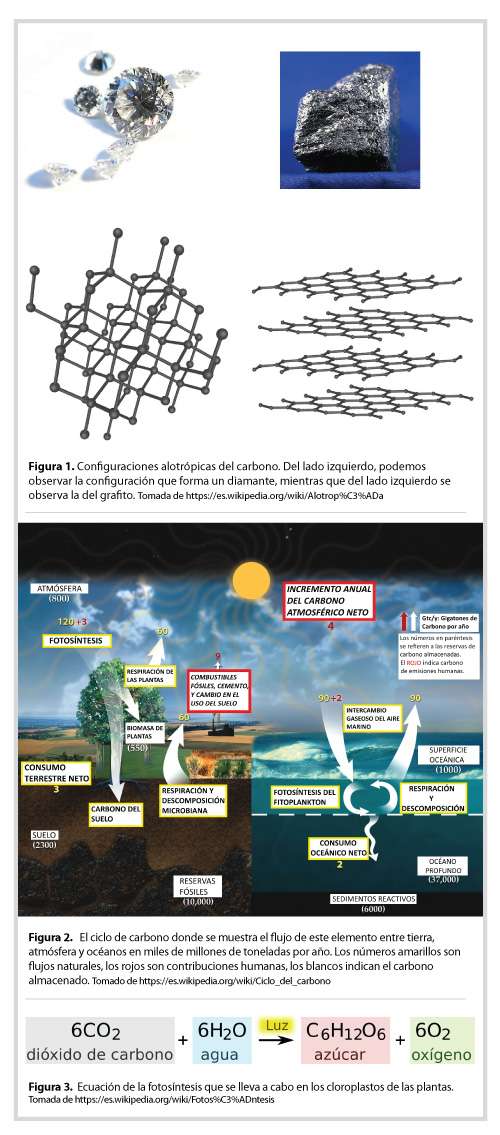
Sin embargo, es interesante que estas rocas en condiciones de alta presión y temperatura, pueden tomar una configuración cristalina la cual conocemos con el nombre de diamante. Estos cristales suelen tener una antigüedad de 2,000 millones de años y a grandes profundidades en la Tierra (~200 km). A diferencia de sus otras formas simples, el diamante es uno de los materiales mas duros del planeta y solo puede ser cortado por otro diamante. Además, debido a su rareza, se le ha dado un valor de gema por un mercado muy exclusivo y controlado. Otra configuración o alótropo del carbono es el grafito, que en realidad es su configuración más estable y que podemos encontrar en cualquier lápiz. La alotropía es la propiedad de algunas sustancias de tener varias estructuras moleculares que les otorgan propiedades físicas diferentes (Figura 1).
En global, el carbono es el 15vo elemento mas abundante en la corteza terrestre y el 4to más abundante a nivel universal (después del hidrogeno), si se considera su masa. Sin embargo, si tomamos en cuenta el carbono que esta formando compuestos orgánicos y gases como el dióxido de carbono (CO2), su abundancia es mayor al menos en nuestro planeta. Aunque el CO2 es un compuesto inorgánico, vamos a tomarlo como punto de partida para hablar de la importancia y versatilidad que tiene el carbono en los seres vivos.
El ciclo del carbono y su importancia para la vida
Este ciclo biogeoquímico es el recorrido que hace este elemento entre la biosfera, que es el conjunto de seres vivos que habitan el planeta; la pedosfera que es la capa mas exterior de la corteza terrestre y esta integrada principalmente por el suelo; la geosfera que es la estructura interna de la Tierra; la hidrósfera que son todos los sistemas acuáticos y finalmente, la atmósfera que es la capa de gases que rodea a nuestro planeta. En este ciclo, podemos estudiar como el carbono se transfiere de tal manera que es reciclado y reusado por la biosfera con lo cual se mantiene la vida (Figura 2).
Algo que es muy importante considerar es el balance global del carbono que es el equilibrio entre los ingresos y perdidas que se dan en el ciclo. Si empezamos por la atmosfera, encontramos al carbono en dos formas principales que son el CO2 y el metano (CH4). En el caso del CO2, podemos observar varios causes en los cuales se utiliza o se mueve este gas. Parte del CO2 se disuelve directamente en los cuerpos de agua o bien, se disuelve con las lluvias. Cuando reacciona con el agua, se forma acido carbónico el cual contribuye al aumento de acidez en el océano, lo cual tiene otros efectos que, aunque no se abordarán aquí, es importante considerar este flujo desde el punto de vista ambiental. En este sentido, tanto el CO2 como el CH4 tienen la propiedad de absorber y retener calor en la atmosfera, por lo que son parte del efecto invernadero. Es por esto que debemos estar conscientes de cuál es la contribución antropogénica en este ciclo y como afecta al clima. En los dos últimos siglos, las actividades humanas han alterado gravemente el ciclo del carbono, y su balance tanto en la corteza como en la atmósfera. Principalmente, hemos visto los cambios más significativos en la atmósfera y a pesar de que los niveles de dióxido de carbono han cambiado naturalmente durante varios miles de años, las emisiones humanas de CO2 han superado las fluctuaciones naturales registradas. Como se mencionó antes, la capacidad de absorber y retener calor de los gases de carbono, es posible comprobar que los cambios en la cantidad de CO2 atmosférico están alterando considerablemente los patrones meteorológicos e indirectamente influyendo la química oceánica. Finalmente, los niveles actuales de CO2 en la atmósfera superan las mediciones de los últimos 420 000 años y de manera muy preocupante, los niveles están aumentando más rápido de lo que jamás se ha registrado. Es por esto que es muy importante entender mejor cómo funciona el ciclo del carbono y cuáles son sus efectos en el fenómeno que hoy conocemos como calentamiento global.
La fotosíntesis: punto de quiebre en la evolución y la vida
Gracias a la fotosíntesis realizada por las plantas, algas y cianobacterias, el CO2 puede dejar la atmosfera he introducirse a la biosfera terrestre y oceánica. La fotosíntesis es el proceso biológico que transforma el CO2 que es un compuesto inorgánico de carbono, en materia orgánica. La reacción química que se lleva a cabo en la fotosíntesis está representada en la Figura 3, donde podemos observar que además se requiere agua y luz para formar oxígeno y uno de los compuestos orgánicos de gran importancia que es la glucosa. Detrás de esta simple reacción, hay millones de años de evolución y aunque la fotosíntesis no es una reacción que estuvo presente en los primeros organismos (bacterias) en el inicio de la vida (http://www.acmor.org.mx/?q=content/el-estudio-del-origen-de-la-vida-un-campo-en-constante-evoluci%C3%B3n), si fue un paso que cambió radicalmente al planeta y la vida como la conocemos.
Los cloroplastos son organelos que podemos encontrar en las células de las plantas, los cuales confinan la maquinaria que se utiliza para llevar a cabo la fotosíntesis. Estas estructuras transforman la energía de la luz en energía y también en diferentes compuestos orgánicos. Si bien, los azúcares como la glucosa y otros compuestos, son de gran importancia en los seres vivos, quisiera hacer referencia en esta ocasión al oxígeno, que es otro de los elementos de los que se hablara en la siguiente entrega. Antes de la fotosíntesis, simplemente no existía el oxígeno y, por lo tanto, muchas de los compuestos de carbono tampoco. Tampoco existía la maquinaria biológica que los sintetiza o al menos no como la observamos actualmente. Incluso, el estado de oxidación de los elementos químicos (esto es que un elemento pierda electrones) era distinto, sobre todo para los metales. Por lo tanto, la aparición del oxígeno en el planeta, no solo afectó el metabolismo de las bacterias que existían antes de su aparición, sino en la gama de compuestos tanto orgánicos como inorgánicos que podemos observar en la actualidad.
La fotosíntesis no solo es importante en la química del carbono, sino que también contribuye a su ciclo removiendo el CO2 de la atmosfera para restaurar parte del balance. Sin embargo, para poder restituir el balance en el ciclo del carbono, no solo bastaría con modificar la biosfera terrestre, sino también controlarlo en otros puntos. El reducir el consumo de compuestos inorgánicos de carbono como son los combustibles fósiles (carbón y petróleo), reducir la generación de metano y no alterar la biosfera marina encargada de realizar fotosíntesis, ayudaría considerablemente a restituir el balance en el ciclo del carbono. Esto tiene que ser un esfuerzo sostenido que posiblemente requiera cientos de años.
La versatilidad del carbono
El carbono es un elemento notable por varias razones. Además de sus formas alotrópicas que incluyen el grafito y el diamante, presenta una gran afinidad para enlazarse químicamente con otros átomos pequeños, incluyendo otros átomos de carbono con los que puede formar largas cadenas. También su pequeño radio atómico le permite formar enlaces múltiples. Así, con el hidrógeno forma numerosos compuestos denominados genéricamente hidrocarburos, esenciales para la industria y el transporte en la forma de combustibles fósiles; y combinado con oxígeno e hidrógeno forma gran variedad de compuestos orgánicos simples como alcoholes, aldehídos y cetonas, o bien algunos más complejos como carbohidratos y ácidos grasos o lípidos. Cuando se incluye al nitrógeno, tenemos otros compuestos como las aminas, amidas e isocianatos que darán origen a otros compuestos más complejos como los aminoácidos que son los bloques básicos de las proteínas, o los nucleótidos que son los bloques básicos del ADN que resguarda la información genética.
La mayoría de los compuestos mencionados anteriormente tienen una configuración lineal, pero parte de la versatilidad del carbono es poder formar compuestos cíclicos. Los compuestos cíclicos o aromáticos, suelen ser muy estables y por lo tanto es más difícil transformarlos. Si consideramos que muchos de los compuestos presentes en el petróleo y sus derivados como los plásticos, tienen una configuración cíclica o aromática, es evidente que su degradación es mucho más difícil, sin mencionar la toxicidad que pueden tener para los seres vivos (http://www.acmor.org.mx/?q=content/pl%C3%A1stico-el-desecho-interminable-%C2%BFjam%C3%A1s-degradable). Si bien la toxicidad del carbono es variable y depende del compuesto del cual forme parte, en general se puede considerar que es baja o casi nula en la mayoría de los casos, sobre todo para aquellos compuestos (biomoléculas) que son sintetizados por organismos vivos. No obstante, la síntesis artificial de compuestos de carbono puede representar un grave problema no solo desde el punto de vista de toxicidad para el humano, sino principalmente para el ambiente ya que, al no existir en la naturaleza, estas moléculas rompen el balance del ciclo del carbono.
Finalmente, si observamos la base de datos más grande de compuestos en la química orgánica (base de datos de Beilstein), podremos encontrar una amplia colección de compuestos orgánicos. Un estudio informático que implico 5.9 millones de sustancias y 6.5 millones de reacciones, demostró que el universo de compuestos orgánicos consiste en una base de alrededor de 200.000 moléculas muy relacionadas entre sí y de una periferia grande (3.6 millones de moléculas) a su alrededor. Desde un punto de vista de redes, la base y la periferia de compuestos están rodeadas por un grupo de pequeñas “islas” no conectadas que contienen 1.2 millones de moléculas, un modelo semejante a la World Wide Web (WWW) o internet. De manera interesante, se considera que es suficiente reconocer cerca de 30 moléculas para tener un conocimiento que permita trabajar con la bioquímica de las células. Dos de esas moléculas son los azúcares glucosa y ribosa; otra, un lípido; otras veinte, los aminoácidos que forman a las proteínas; y cinco las bases nitrogenadas que son parte de los nucleótidos que forman el ADN.
Con estas y otras evidencias, espero que el lector note la importancia del carbono y otros compuestos que se abordaran en detalle en las siguientes entregas.
El 2019 ha sido propuesto por la Organización de las Naciones Unidas como el Año Internacional de la Tabla Periódica de los Elementos por lo que la Academia de Ciencias de Morelos ha decidido dedicarle una serie de artículos preparados por especialistas de diferentes disciplinas. Sirva este artículo para despertar su curiosidad y que nos permitan compartir con ustedes nuestro amor por los elementos y su máxima representación, la Tabla Periódica.
Esta columna se prepara y edita semana con semana, en conjunto con investigadores morelenses convencidos del valor del conocimiento científico para el desarrollo social y económico de Morelos. Desde la Academia de Ciencias de Morelos externamos nuestra preocupación por el vacío que genera la extinción de la Secretaría de Innovación, Ciencia y Tecnología dentro del ecosistema de innovación estatal que se debilita sin la participación del Gobierno del Estado.
Referencias:
https://es.wikipedia.org/wiki/Carbono
https://es.wikipedia.org/wiki/Ciclo_del_carbono
https://es.wikipedia.org/wiki/Fotos%C3%ADntesis
Fuente: Academia de Ciencias de Morelos