Prueban con éxito en una niña una nueva terapia contra las infecciones bacterianas resistentes
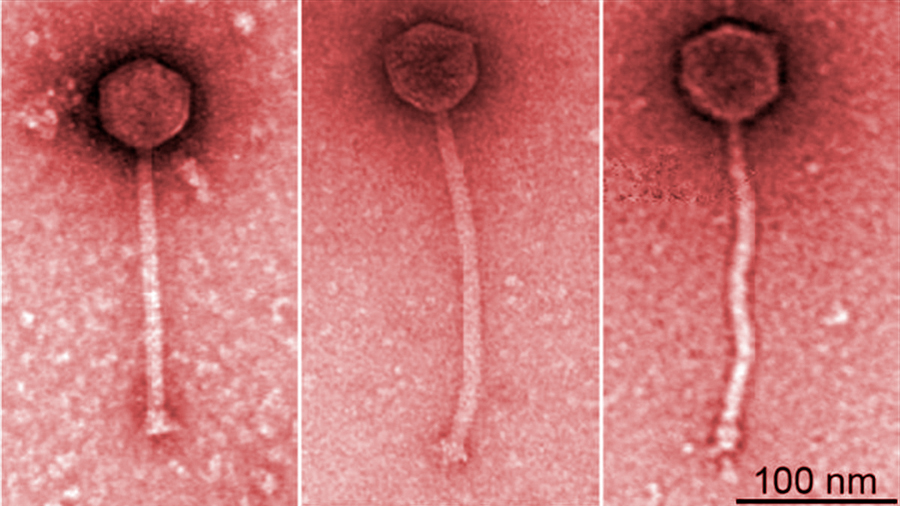
Investigadores han usado una terapia experimental que depende de virus que infectan bacterias. La han probado en una paciente, una niña de 15 años, que había acudido al ‘Great Ormond Street Hospital’ de Londres, en Reino Unido, para un trasplante doble de pulmón.
Era el verano de 2017, y sus pulmones luchaban por alcanzar incluso un tercio de su función normal. Tenía fibrosis quística, una enfermedad genética que obstruye los pulmones con moco y plaga a los pacientes con infecciones persistentes. Durante ocho años, había estado tomando antibióticos para controlar dos cepas bacterianas persistentes.
Semanas después del trasplante, los médicos notaron enrojecimiento en el sitio de la herida quirúrgica y signos de infección en el hígado. Luego, vieron nódulos (bolsas de bacterias que empujaban hacia arriba a través de la piel) en sus brazos, piernas y glúteos. La infección de la niña se había extendido y los antibióticos tradicionales ya no funcionaban.
Ahora, un nuevo tratamiento personalizado está ayudando a la niña a sanar. El tratamiento se basa en bacteriófagos genéticamente modificados, virus que pueden infectar y matar las bacterias. Durante los siguientes seis meses, casi todos los nódulos cutáneos de la niña desaparecieron, su herida quirúrgica comenzó a cerrarse y su función hepática mejoró, según informan los científicos en un artículo publicado este miércoles en la revista ‘Nature Medicine’.
El trabajo es el primero en demostrar el uso seguro y eficaz de bacteriófagos diseñados en un paciente humano, dice Graham Hatfull, profesor del Instituto Médico Howard Hughes (HHMI, por sus siglas en inglés) en la Universidad de Pittsburgh, Estados Unidos. Dicho tratamiento podría ofrecer un enfoque personalizado para contrarrestar las bacterias resistentes a los medicamentos e, incluso, podría potencialmente usarse más ampliamente para controlar patologías como la tuberculosis. «La idea es usar los bacteriófagos como antibióticos, como algo que podríamos emplear para matar las bacterias que causan una infección», afirma Hatfull.
En octubre de 2017, Hatfull recibió el correo electrónico que llevó a su equipo en una búsqueda de bacteriófagos de un mes de duración. Un colega en el Hospital de Londres presentó el caso: dos pacientes, ambos adolescentes. Ambos tenían fibrosis quística y habían recibido trasplantes de doble pulmón para ayudar a restaurar la función pulmonar. Ambos habían sido infectados crónicamente con cepas de ‘Mycobacterium’, parientes de la bacteria que causa la tuberculosis.
Las infecciones se habían resuelto hace años y se habían inflamado después del trasplante. «Estos insectos no respondieron a los antibióticos –relata Hatfull–. Son cepas de bacterias altamente resistentes a los medicamentos». Pero tal vez algo más podría ayudar. Hatfull, genetista molecular, había pasado más de tres décadas acumulando una colosal colección de bacteriófagos, o fagos, del medio ambiente. El colega de Hatfull se preguntó si alguno de estos fagos podría atacar las cepas de los pacientes.
Fue una idea imaginativa, recuerda Hatfull, y estaba intrigado. Su colección de fagos, la más grande del mundo, residía en aproximadamente 15.000 frascos y llenaba los estantes de dos congeladores de seis pies de altura en su laboratorio. Habían sido recolectados en miles de lugares diferentes en todo el mundo, y en gran parte por estudiantes.
Hatfull dirige un programa de HHMI llamado SEA-PHAGES que ofrece a los estudiantes de primer año de la universidad y de segundo año la oportunidad de recoger fagos. En 2018, casi 120 universidades y colegios y 4.500 estudiantes en todo el país participaron en el programa, que involucró a más de 20.000 estudiantes en la última década.
En la tierra, el agua y el aire hay más de un billón de veces el cuatrillón de fagos. Después de probar muestras para encontrar un fago, los estudiantes lo evalúan. Verán cómo se ve bajo un microscopio electrónico, secuenciarán su genoma, probarán cómo de bien infecta y mata a las bacterias, y averiguarán dónde encaja en el árbol genealógico del fago.
«Este programa involucra a estudiantes principiantes en ciencias reales –dice David Asai, director senior de educación en Ciencias del HHMI y director del programa SEA-PHAGES–. Lo que descubran es nueva información». Esa información biológica básica es valiosa, considera. «Ahora la colección de fagos ha contribuido realmente a ayudar a un paciente», añade.
Esa no era la intención original del programa, explican Asai y Hatfull. «Tenía la sensación de que esta colección era enormemente poderosa para abordar todo tipo de preguntas en biología –afirma Hatfull–. Pero no pensamos que alguna vez llegaríamos a un punto de usar estos fagos terapéuticamente».
Terapia experimental
La idea de la terapia con fagos ha existido durante casi un siglo. Pero hasta hace poco, no había mucha información sobre la seguridad y la eficacia del tratamiento. En 2017, médicos de San Diego, California (Estados Unidos), utilizaron con éxito fagos para tratar a un paciente con una bacteria resistente a múltiples fármacos. Ese caso, y el incremento de la resistencia a los antibióticos, ha alimentado el interés en los fagos, dice Hatfull.
Menos de un mes después de que se enteró de los dos pacientes infectados en Londres, recibió muestras de sus cepas bacterianas. Su equipo buscó en su colección los fagos que podrían atacar estas bacterias. Probaron fagos individuales que se sabe que infectan a parientes bacterianos de las cepas de los pacientes, mezclaron miles de otros fagos y probaron el lote.
Estaban buscando algo que pudiera eliminar la película blanquecina de bacterias que crecen en platos de plástico en el laboratorio. Si un fago pudiera hacer eso, razonó el equipo, podría combatir las infecciones de los pacientes. A fines de enero, el equipo encontró un ganador, un fago que podría afectar a la tensión que infectó a uno de los adolescentes, pero llegaron demasiado tarde, dice Hatfull. Uno de los pacientes había muerto ese mismo mes. «Estas realmente son infecciones graves que amenazan la vida», dice.
Sin embargo, su equipo tenía algunas pistas para el segundo paciente: tres fagos, llamados Muddy, ZoeJ y BPs. Muddy podía infectar y matar las bacterias de la niña, pero ZoeJ y BP no eran tan eficientes. Así que Hatfull y sus colegas modificaron los genomas de los dos fagos para convertirlos en asesinos de bacterias. Eliminaron un gen que permite que los fagos se reproduzcan sin causar daño dentro de una célula bacteriana. Sin el gen, los fagos se reproducen y estallan desde la célula, destruyéndolo. Luego combinaron el trío en un cóctel de fagos, lo purificaron y lo probaron para garantizar su seguridad.
En junio de 2018, los médicos administraron el cóctel a la paciente por vía intravenosa dos veces al día con mil millones de partículas de fago en cada dosis. Después de seis semanas, una exploración del hígado reveló que la infección había desaparecido esencialmente. Hoy la niña solo tiene uno o dos nódulos cutáneos. Hatfull tiene grandes esperanzas: las bacterias no han mostrado ningún signo de desarrollo de resistencia a los fagos, y su equipo ha preparado un cuarto fago para agregar a la mezcla.
Identificar los fagos adecuados para cada paciente es un gran desafío, dice Hatfull. Un día, los científicos podrán elaborar un cóctel de fagos que funciona más ampliamente para tratar enfermedades, como las infecciones por ‘Pseudomonas’ que amenazan a los pacientes con quemaduras. «Estamos en un territorio desconocido», afirma, agregando que los fundamentos del caso de la joven son bastante simples. «Purificamos los fagos, se los dimos a la paciente y la paciente mejoró», resume.
Fuente: infosalus.com