Los pacientes de párkinson que toman el fármaco levodopa, o L-DOPA, siempre acaban decepcionados. Al principio, durante un período de «luna de miel», consigue controlar sus síntomas (que incluyen temblores y problemas de equilibrio), pero con el paso del tiempo el fármaco pierde eficacia. Esto les obliga a recurrir a dosis muy altas y algunos incluso acaban pasando varias horas al día en un estado de parálisis casi total.
Pero una empresa de biotecnología llamada Voyager Therapeutics cree que puede ampliar los efectos de L-DOPA con un enfoque sorprendente: la terapia génica. La empresa, con sede en Cambridge (EU), está probando la idea en pacientes de párkinson que han accedido a someterse a una cirugía cerebral y una inyección de ADN nuevo.
La enfermedad de Parkinson se produce cuando las neuronas productoras de dopamina empiezan a morir, lo que provoca los síntomas de movimiento que afectaron al campeón de boxeo Muhammad Ali y al actor Michael J. Fox, cuya organización benéfica ha ayudado a financiar el desarrollo del tratamiento experimental de Voyager Therapeutics.
Las causas del párkinson no están claras, pero el motivo por el que los efectos del fármaco se desvanecen sí. Se debe a que el cerebro también empieza a perder la enzima conocida como L-aminoácido aromático descarboxilasa (AAAD) que necesita para convertir la L-DOPA en dopamina.
La estrategia de Voyager Therapeutics, que ha empezado a probar con pacientes en un pequeño estudio, consiste en inyectar virus que entreguen el gen de la AAAD al cerebro. Esta idea podría hacer retroceder el reloj de forma que la L-DOPA empiece a funcionar de nuevo en pacientes de párkinson.
Los vídeos de pacientes antes y después de tomar L-DOPA dejan claro por qué querrían que el fármaco funcione con dosis más bajas. En el estado «latente», los pacientes se mueven a cámara lenta. Tocarse la nariz es todo un esfuerzo. En un estado «activo», cuando funciona el fármaco, tiemblan pero no están tan severamente discapacitados.
«Van bien al principio pero después responden de forma muy errática a la L-DOPA», afirma el científico de la Universidad de California (UC, en EU) que elaboró el plan para la terapia génica y el cofundador de Voyager Therapeutics, Krystof Bankiewicz. «Este ensayo busca restaurar la enzima y permitir que [los pacientes] se encuentren en estado ‘activo’ durante períodos de tiempo más largos», añade.
Voyager Therapeutics se fundó en 2013 y después realizó una OPI en la que recaudó alrededor de unos 76 millones de euros. La empresa forma parte de una creciente oleada de empresas de biotecnología capaces de recaudar dinero para terapias génicas, una tecnología que empieza a generar beneficios. Tras tres décadas de investigaciones, unos pocos productos ya están empezando a llegar al mercado.
A diferencia de los estudios farmacológicos convencionales, los que incluyen la terapia génica a menudo se asocian a unas altísimas expectativas de que el tratamiento funcione, pues están diseñados para corregir errores de ADN para los que se conocen las consecuencias biológicas exactas. Genzyme, una unidad del fabricante farmacéutico europeo Sanofi, pagó a Voyager Therapeutics casi 60 millones de euros y prometió aportar cientos de millones más a cambio de los derechos de comercialización en Europa y Asia de cualquier tratamiento que desarrolle.
El CEO de Voyager Therapeutics, Steven Paul explica: «Trabajamos de acuerdo a 60 años de farmacología de dopamina. Si logramos proporcionar el gen correcto al tejido correcto en el momento correcto, lo raro sería que no funcionara».
Pero hay muchas excepciones. De hecho, el concepto de la terapia génica para tratar el párkinson data de 1986, cuando Bankiewicz determinó que la escasez de AAAD provoca la pérdida de eficacia de la L-DOPA. Creía que la terapia génica podría solucionarlo, pero no fue hasta 20 años después cuando pudo probar la idea en pacientes en un estudio dirigido por la UC en San Francisco (EU).
Según Bankiewicz, en ese ensayo la entrega genética no fue tan exitosa como se había esperado. No se actualizaron suficientes células cerebrales con la nueva información genética entregada por los virus inyectados al cerebro. Los pacientes parecían mejorar, pero no demasiado.
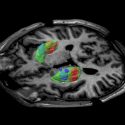
Aunque el tratamiento no salió según lo previsto, ese primer estudio remarcó una ventaja del enfoque de Voyager Therapeutics frente a los demás: es posible etiquetar la AAAD con un marcador químico de forma que permite a los médicos realmente observar su rendimiento dentro de los cerebros de los pacientes. De hecho, la producción continua de la enzima generadora de dopamina aún sigue siendo visible dentro de los cerebros de los pacientes de la UC varios años después.
En algunos estudios anteriores con terapias génicas, en cambio, los médicos tuvieron que esperar a que fallecieran los pacientes para averiguar si el tratamiento había sido correctamente entregado. Paul detalla: «Esto es un tratamiento de aplicación única y revela automáticamente si lo hemos entregado en el sitio correcto».
Un nuevo ensayo en curso, esta vez dirigido por Voyager Therapeutics, está diseñado para introducir niveles mucho más altos de ADN en los cerebros de los pacientes con la esperanza de lograr mejores resultados. Para ello, Bankiewicz desarrolló un sistema para inyectar las partículas virales cargadas de genes mediante tubos presurizados mientras el paciente reposa dentro de un escáner de resonancia magnética. De esta manera el cirujano puede observar el directamente la región del cerebro a la que se intenta dirigir el ADN, para asegurarse de que sea cubierta por el tratamiento.
Existen otras terapias génicas para tratar el párkinson en fase de planificación o de prueba. Un ensayo desarrollado por los Institutos Nacionales de Salud de Estados Unidos busca añadir un factor de crecimiento y regenerar células. Una empresa europea, Oxford BioMedica, intenta reemplazar la dopamina.
En total, a fecha de este año había 48 ensayos clínicos en curso de sustitución génica o celular en el cerebro y el sistema nervioso, según la Alianza para la Medicina Regenerativa, un grupo comercial. El sistema nervioso es el cuarto objetivo más común para este tipo de tratamientos experimentales, después del cáncer, las enfermedades cardiovasculares y las infecciones.
La plantilla de Voyager Therapeutics está especialmente motivada conun participante del estudio al que llaman «el paciente número seis». Llevan meses siguiéndole desde que recibió el tratamiento. Antes de la terapia génica, recibía una alta dosis de L-DOPA pero aún así pasaba seis horas al día en estado latente. Ahora ese período se ha reducido a dos horas al día y el paciente recibe una dosis más baja del fármaco.
El paciente número seis recibió la dosis más alta de ADN que se ha administrado hasta la fecha, que cubrió la mayor área del cerebro. En parte, esto es lo que hace que Voyager Therapeutics crea que unas dosis más altas deberían ser eficaces. Bankiewicz concluye: «Creo que el fracaso anterior de los ensayos de terapia génica para el párkinson se debió a una entrega subóptima».
Fuente: Technologyreview.es