Carol Perelman
Es Química Farmacéutica Bióloga por la UNAM y Divulgadora de la Ciencia. Ganadora de Medallas de Oro y Bronce en las Olimpiadas de Química Nacional e Iberoamericana representando a México, es co-creadora y directora del Jardín Weizmann de Ciencias, primer museo de ciencias completamente al aire libre en México. En 2019 ganó 3er Lugar en Periodismo de Ciencia por Comecyt y en 2021 obtuvo el 2o Lugar del Premio Jorge Flores Valdés al mejor producto de divulgación en torno a la Pandemia por su cuento “Coronesio, Covidin y los Secretos de lo Invisible”. Es investigadora, conferencista, columnista, colaboradora de varios medios, miembro de RedMPC y Somedicyt. Es esposa y mamá.
Esta publicación fue revisada por el comité editorial de la Academia de Ciencias de Morelos.
Los premios Nobel se anuncian en octubre
Eran las 3:45 a.m. cuando a las afueras de Filadelfia sonó el teléfono en casa de la bioquímica húngara-americana Katalin Karikó. La llamada madrugadora ese 2 de octubre le dio la noticia de que junto con el inmunólogo Drew Weissman recibiría el Premio Nobel de Fisiología o Medicina de 2023. Inicialmente pensó que era una broma y texteó a su colega para ver si también le habían llamado. Incrédulos, decidieron esperar sentados en sus respectivas camas hasta que desde Estocolmo escucharan el anuncio oficial. Aunque quienes fuimos testigos de la maravilla de su invento ansiábamos que el dúo recibiera este galardón, ellos confiesan que no se lo esperaban.
Este año, la Asamblea del Nobel del Instituto Karolinska los decidió reconocer por “su descubrimiento en la modificación de bases de nucleósidos que permitieron el desarrollo de vacunas efectivas de ARNm (ácido ribonucleico mensajero) contra COVID-19”. Es decir, tal como Alfred Nobel estipuló en su testamento, se premiaría un hallazgo “en beneficio de la humanidad”. Porque si leemos entre líneas, realmente este galardón no se limita a haber realizado rápidamente vacunas seguras y eficaces para dejar atrás la peor pandemia de los últimos años; Karikó y Weissman descubrieron una nueva forma de hacer gran diversidad de vacunas y tratamientos para enfermedades que hoy no tienen cura. La pandemia fue la primera puesta en escena.
Horas más tarde, ese mismo 2 de octubre, la Universidad de Pensilvania (UPenn) ofreció una conferencia de prensa (Figura 1) [1] en la cual, al lado de Drew Weissman, Katalin Karikó mencionó que hay ya más de 200 ensayos clínicos en curso usando el ARNm como estrategia preventiva, de tratamiento o diagnóstica. Así que la revolución apenas está comenzando y las aplicaciones de esta nueva tecnología trascienden más allá de lo que hemos atestiguado. Es evidente que el éxito durante la pandemia por COVID-19 visibilizó y aceleró el apoyo al ARNm, pero lo que es increíble es que este premio está dándose a escasos 3 años de haberla implementado por primera vez; generalmente pasa una década para que se dé el Nobel a un hallazgo, dando oportunidad a que madure y confirme sus beneficios, pero esta vez, como lo dijo Drew Weissman, el Comité del Nobel a través de su secretario general, le dijo que este año querían ser “actuales”.

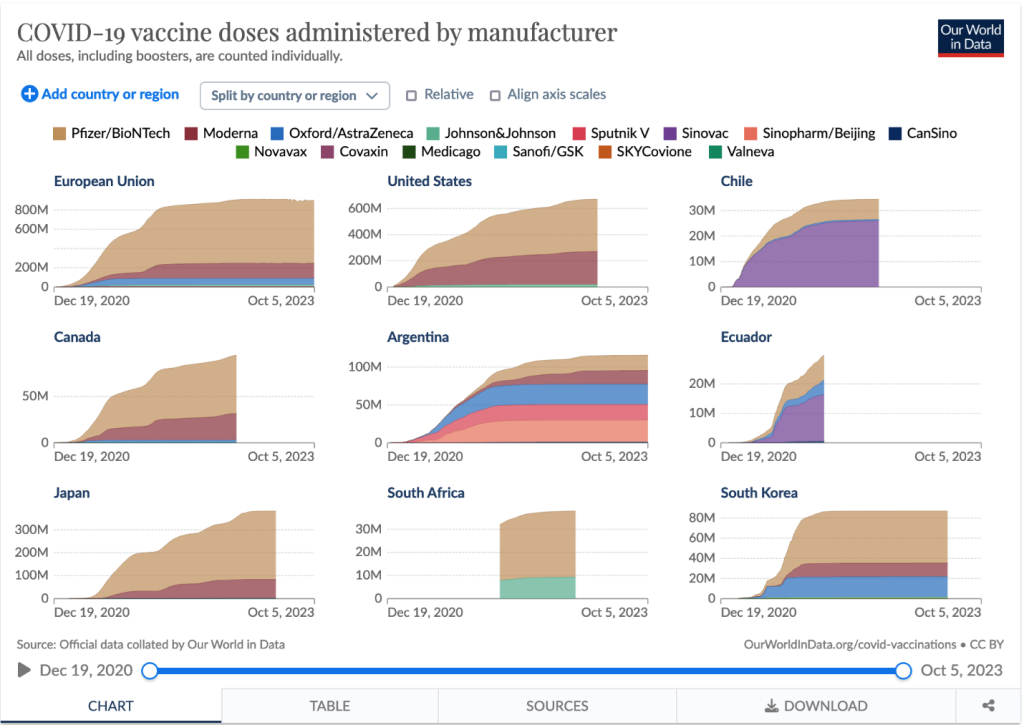
Recordemos que, en 2020, las vacunas de ARNm en sus resultados de estudios clínicos de fase 3 mostraron, a la vez de ser seguras, una sorprendente eficacia de 95% para reducir infecciones, complicaciones y muertes por COVID-19. Y luego de miles de millones de dosis aplicadas, siendo una gran proporción las de Pfizer-BioNTech y Moderna de ARNm (Figura 2), un estudio publicado en The Lancet en 2022 por el Imperial College de Londres [2] calculó que en 2021 las vacunas contra COVID-19 evitaron al menos 20 millones de muertes en el mundo. No por nada el texto que esa misma tarde publiqué, llevó por título “Un Premio Nobel de Medicina que podría también ser de la Paz” [3].
El principio de la historia
Y es que, en realidad, la historia del ARNm comenzó mucho antes que todo esto. En 1985, Katalin Karikó, nacida treinta años antes en Hungría, en una casa sin televisión, agua corriente ni refrigerador, de padre carnicero y madre bibliotecaria, migró a Estados Unidos con su esposo y su hija, Susan Francia, futura medallista olímpica en remo. Dada la situación política en su país natal, Karikó tuvo que esconder en el peluche de Susan las 900 libras que cobró en el mercado negro por vender su auto. Una vez establecida en la Universidad de Temple, Karikó trabajó con ARN de doble hebra como terapias para HIV y fatiga crónica, experiencia que le hizo pensar en las múltiples posibilidades del ARNm. Desde entonces, y a partir de 1988 que se integró a UPenn, Kati, como le dicen sus amigos, se enfocó en el ARNm como una probable terapia génica; el gran problema era que nadie más le veía potencial. Aunque apoyada siempre por su hija y esposo, estaba sola en esta misión idealista que parecía inalcanzable y poco relevante. No recibía apoyos, e incluso UPenn amenazaba con retrasarla en su carrera.
Karikó no conseguía financiamiento, pero era sumamente estudiosa, y la perseverancia y el amor por su trabajo hizo que, a pesar de todo, no quitara la vista de su objetivo. Finalmente, en 1997 Karikó conoció frente a la fotocopiadora Xerox de UPenn, al inmunólogo Drew Weissman. Un encuentro fortuito dado que además de que trabajaban en edificios distintos, no pertenecían al mismo departamento. El entusiasmo científico de Karikó y el interés de Weissman hicieron que emprendieran un proyecto conjunto que comenzó a tomar forma, se hizo factible y que hoy culmina con el máximo galardón.
El ARNm es una molécula esencial en el envío de información ubicada en el DNA para la elaboración de proteínas en los ribosomas, siendo así una especie de telegrama entre las instrucciones guardadas en la bóveda genética celular y la fábrica proteica ubicada en el citoplasma, pero, aunque el ARNm había sido descubierto desde 1961, no se había vislumbrado su eventual uso farmacológico. La presidenta de UPenn, Elizabeth Magill, describió con asertividad las 4 características del carácter que catalizaron el gran aporte de los investigadores: su curiosidad, su tenacidad, su creatividad y su dedicación por el beneficio colectivo. Es evidente que para apreciar un avance científico tan extraordinario como el uso de ARNm para evitar, detectar y tratar enfermedades, hay que reconocer el arduo e innovador trabajo de las personas tras de él. Los momentos de éxito y también los matices de dificultad. La obra maestra no puede disociarse de su alfarero.
Los retos que este par de científicos enfrentó no sólo se limitaron a los económicos y al gran escepticismo de sus colegas, también hubo enigmáticos rompecabezas técnicos que tuvieron que resolver usando su máximo ingenio. “99% de la ciencia es un reto”, admitió Karikó, “estás haciendo cosas que nunca has hecho o que nadie ha hecho, y ni si quiera sabes si es posible hacerlo”. A pesar de que el ARNm está hecho de sólo 4 bases nitrogenadas (representadas en 4 letras: A=adenina, U=uracilo, C=citosina, G=guanina) haciéndolo muy sencillo de modificar, es una molécula que presentaba primordialmente dos limitaciones; es sumamente lábil, por lo que Drew y Katalin tuvieron que eventualmente aliarse con los creadores de nanopartículas de lípidos para protegerlo y garantizar su estabilidad, y el ARNm que usaban en los experimentos in vitro provocaba una reacción inflamatoria, obstáculo que nublaba la posibilidad de usarse como terapia, pero que pudo ser esquivado gracias a una brillante observación.
Weissman, quien trabajaba con las células dendríticas responsables de la respuesta inmunológica innata encontró, junto con Karikó, que estas células reconocían al ARNm que usaban como extraño, limitando por ello la posibilidad de uso en estrategias terapéuticas, pero estas mismas células inmunológicas no presentaban respuesta frente al ARNt (ácido ribonucleico de transferencia), un primo hermano del ARNm. Obviamente había que entender qué hacía diferente al ARNm y al ARNt, en ello residía el futuro del ARNm como terapia. Al analizar esta extraña situación, Drew y Katalin descubrieron que el ARNt tenía un nucleósido modificado en su estructura, una pseudouridina en vez de la uridina (U) tradicional. Alentador y emocionante. Así, al colocar la pseudouridina en vez de la uridina en el ARNm se suprimía la respuesta inmune y las células dendríticas ya no montaban una reacción inflamatoria. Este bellísimo hallazgo, hoy premiado con un Nobel [4] lo anunciaron Karikó y Weissman en 2005 en la revista Immunity [5] luego de que las prestigiosas Science y Nature rechazaron su publicación. Con esta sustitución de nucleósidos se abría, ahora sí, la posibilidad de usar el ARNm como estrategia terapéutica. Y así fue.
Una nueva estrategia
Aunque lo que siguió se convirtió en más investigación, en patentes, licencias, empresas, inversiones y sueños, muchos seguían ignorando al ARNm. Lo que sí es que quienes sí pusieron especial atención a esta oportunidad comenzaron a trabajar para saber más, robustecer el conocimiento y construir evidencia sólida, y desde antes de que se declarara la emergencia por la pandemia de COVID-19 en 2020, la empresa BioNTech ya trabajaba con Pfizer en el desarrollo de una posible vacuna de ARNm contra Influenza. Por su parte, Moderna pensaba en productos inmuno-oncológicos a base de ARNm y la alemana CureVac diseñaba ARNm contra el cáncer. Ninguno había terminado fases clínicas, todas seguían en experimentación, pero el camino estaba ya bastante pavimentado.
Es por todo esto, y por ser el ARNm una plantilla sumamente sencilla de modificar, que cuando la amenaza por el nuevo coronavirus requirió que los esfuerzos científicos y farmacéuticos se enfoquen en salvar vidas y sacar al mundo de la agobiante parálisis, se pudieron tener las vacunas contra COVID-19 en menos de 10 meses. Y sí, claro que fue rápido; habitualmente la vacuna contra un nuevo patógeno tarda en promedio 8 años para desarrollarse desde su diseño, pasando por las etapas preclínicas y clínicas, hasta su producción y autorización. Y aunque justamente el haberlas tenido en tiempo récord se usó por grupos anti-vacunas como estandarte para sembrar dudas, llevaban ya las vacunas de ARNm 30 años de gestación; tres décadas de trabajo riguroso para su exitosa elaboración. Al no requerir cultivos celulares y ser tan fácil de modificar, el uso de ARNm es ágil y adaptable, rompiendo con ello los paradigmas de tiempo establecidos por tecnologías tradicionales como las inactivadas, atenuadas, de vector viral, proteicas y de ADN.
Al día de hoy aún no podemos dimensionar las vastas posibilidades del uso de ARNm, sólo el futuro nos dirá, pero por lo pronto está en proceso de estudio en las vacunas contra citomegalovirus, Zika, Virus Respiratorio Sincicial, Influenza, Rabia, Chikungunya; contra cánceres como gastrointestinales, de mama, de ovario, por virus de papiloma humano, melanoma; en uso como terapias génicas según las características de los tumores; contra enfermedades metabólicas, infarto al miocardio o fibrosis quística, contra autoinmunes como artritis reumatoide, contra alergias, entre muchas otras aplicaciones.
Una sorpresa para mi
Así, a la media noche de ese mismo 2 de octubre, revisé antes de dormir mi cuenta de Instagram [6] y con sorpresa descubrí que la mismísima Karikó había reposteado el story que unas horas antes subí comunicando la gran noticia, y por si no fuera suficiente, dos días después, debajo del post que compartí, Karikó me escribió un comentario: “Thank you” seguido de 4 corazones (Figura 3). Imposible describir con palabras mi sentimiento, sigo sumamente conmovida. Si esta gran científica, habiendo navegado las hostilidades de su trayectoria para convertirse en la 13ava mujer en ganar el Premio Nobel de Medicina ya era una inspiración, ahora vi en ella y de primera mano, sus cualidades humanas: a pesar del reflector y la premura de tiempo, demostró su gratitud y generosidad, acrecentando hasta el infinito mi profunda admiración por su trabajo, pero especialmente por ella. Si hubiera suficiente espacio para colocar todos los caracteres le contestaría “Thank you to you Katalin” seguido de casi 8 mil millones de corazones.

Y es que Katalin aprendió a no distraerse por los obstáculos y más bien destinar su tiempo y energía en cómo hacer que las cosas ocurran, una enseñanza inspiradora para quien sea en el área que sea. “Cuando algo no está disponible, no te das por vencido, creas algo tú; porque si quieres lograr algo, encuentras la manera.” Y sin duda ella lo ha logrado, y además combinándolo con su rol de madre y de esposa. “Consigan un esposo que las apoye,” recomienda a las mujeres que buscan una carrera en la ciencia. Su meta desde chica fue ser científica, aunque nunca había conocido a una. Incluso desde la primaria mostró interés al ganar tercer lugar en un concurso de biología en Hungría, pero admite que nunca consideró que iba a recibir premios, aplausos o reconocimientos.
El camino de la ciencia
Con su humildad, gran honestidad y sentido del humor, Karikó recomendó en la conferencia de prensa de UPenn “disfrutar siempre lo que hagas”, tal como lo ha hecho ella, y advirtió: “si quieres destacar, conviértete en actor; si quieres seguir instrucciones, enlístate en el ejército; si quieres hacerte rico, no tengo ni idea qué hacer; pero si quieres resolver problemas, busca el camino de la ciencia.” En este mismo sentido, Drew Weissman afirmó dirigiéndose a los jóvenes: “la ciencia ha cambiado la historia de la humanidad, desde la invención de la rueda hasta el día de hoy.”
Una mujer, cuya madre hasta antes de morir en 2018, escuchaba cada año los anuncios del Nobel esperando oír el nombre de su hija, es hoy la que nos enseña que “cuando fracasas debes enfocarte en lo que sí puedes cambiar.” Y ella, la madre del ARNm, tras múltiples fracasos lo que sí pudo cambiar, es al mundo.
Referencias
https://penntoday.upenn.edu/news/wrong-number-cryptic-message-and-big-win-nobel-weissman-kariko
(2) Watson OJ, Barnsley G, Toor J, Hogan AB, Winskill P, Ghani AC. Global impact of the first year of COVID-19 vaccination: a mathematical modelling study. Lancet Infect Dis. 2022 Sep;22(9):1293-1302. doi: 10.1016/S1473-3099(22)00320-6.
https://www.carolperelman.net/post/un-premio-nobel-de-medicina-que-podr%C3%ADa-tambi%C3%A9n-ser-de-paz
https://www.nobelprize.org/prizes/medicine/2023/press-release/
Karikó, K., Buckstein, M., Ni, H. and Weissman, D. Suppression of RNA Recognition by Toll-like Receptors: The impact of nucleoside modification and the evolutionary origin of RNA. Immunity 23, 165–175 (2005)
https://www.instagram.com/p/Cx6ToVvSQ-d/?igshid=MzRlODBiNWFlZA==
Fuente: acmor.org

