El futuro de los biomateriales en México
Juan V. Cauich Rodríguez
Unidad de Materiales, Centro de Investigación Científica de Yucatán A.C.
jvcr@cicy.mx
En 2002 fui invitado por la Sociedad Polimérica de México a escribir sobre los biomateriales en México y, desde entonces, siento que mucho ha cambiado motivándome a reflexionar sobre esta situación. Este escrito solo tiene por fin reflexionar sobre el área y decir que no existe el padre o la madre de los biomateriales en México. Todos contribuimos con un poco cada día.
Comenzando por el principio
Un biomaterial fue definido en 1991 como un material con la intención de interactuar con sistemas biológicos para evaluar, tratar, aumentar o sustituir cualquier tejido, órgano o función en el cuerpo1. Debido a las limitaciones en esta definición, con el paso de los años una nueva definición fue acuñada en 2009, la cual lo define como “una sustancia que ha sido diseñada mediante ingeniería para tomar una forma, la cual sola o como parte de un sistema complejo, es usada para dirigir, mediante el control de ciertas interacciones con los componentes de sistemas vivos, el curso de un procedimiento de diagnóstico o terapéutico, en seres humanos o medicina veterinaria”2.
Después de la reunión de Chester, UK en 1986, la biocompatibilidad fue definida como la capacidad de un biomaterial para desempeñarse con una respuesta del huésped adecuada en una aplicación específica. Sin embargo, esta definición no especifica cómo evaluar o, mejor aún, como mejorarla. Por lo tanto, esta definición fue mejorada incluyendo el desempeño de una función con respecto a una terapia médica, sin provocar una respuesta local o sistémica indeseable pero generando la mejor respuesta celular o tisular. En general, la biocompatibilidad puede ser vista como una reacción a un cuerpo extraño en tejidos vascularizados. Sin embargo, recientemente se ha propuesto que la biocompatibilidad es la habilidad de un biomaterial para disparar y guiar de manera local una cicatrización no fibrótica, y la reconstrucción e integración tisular. Esta nueva definición es altamente contrastante con lo observado actualmente, en donde un mejor concepto es la biotolerabilidad, entendida como la habilidad de un material para residir en el cuerpo por periodos largos con una reacción inflamatoria de bajo nivel3.
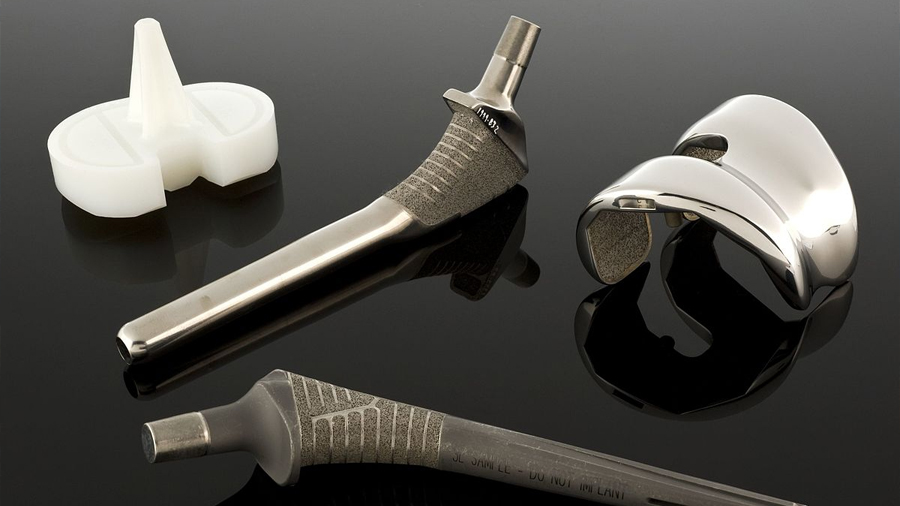
De este modo, los biomateriales tradicionales metálicos pueden ser usados, en ortopedia y estomatología, como implantes, siendo muy difícil que estos sean reemplazados a corto plazo por elementos no metálicos, incluyendo a los materiales compuestos. Por su parte, los materiales cerámicos a base de alumina o circonia son útiles en ortopedia como cabezas femorales, mientras que la hidroxiapatita, el β-TCP, α-TCP e, incluso, sulfatos de calcio se usan en aplicaciones dentales como injertos óseos. Por su parte los polímeros, debido a su baja densidad, capacidad de adquirir distintas geometrías y prestaciones mecánicas, se han empleado en aplicaciones ortopédicas, dentales y como sustitutos de tejidos blandos (injertos cardiovasculares, tráqueas, válvulas cardíacas, etc.). Cuando los polímeros son hidrofílicos y tienen la capacidad de formar hidrogeles, sus aplicaciones pueden extenderse a sustitutos de tejido blando, por ejemplo, cartílago articular y en la liberación controlada de fármacos o cualquier principio activo. Como muy pocas veces, las propiedades de los polímeros solos proporcionan todas las propiedades deseables, se sugiere su combinación con materiales cerámicos. Para la sustitución de tejido duro es común usar HA, fosfatos de calcio con razones Ca/P variables, biovidrios, etc. que proporcionen osteoconducción u osteoinducción. La figura 1 ilustra algunas de estas aplicaciones.
¿Dónde estamos actualmente?
Hace 15 años, los biomateriales estaban clasificados como metales, cerámicos, polímeros o materiales compuestos, siendo todos ellos principalmente bioestables. Ahora, se habla un lenguaje diferente, por ejemplo, metales biodegradables base de magnesio, vidrios bioactivos no sólo a base de silicatos sino de boratos y dopados con distintos elementos traza para otorgarles propiedades específicas; los cerámicos ya no sólo son bioinertes, como la circonia o alumina, sino bioactivos. Los materiales compuestos ahora son a base de nanocelulosas cristalinas, nanotubos de carbono funcionalizados o grafenos oxidados o incluso, materiales híbridos orgánicos-inorgánicos. Los polímeros principalmente son biodegradables para ser usados como soportes en ingeniería tisular y no sólo a base de policaprolactona, poli(ácido láctico), poli(ácido glicólico) o sus copolímeros, sino también a base de polifosfacenos, polidioxanona, polianhídridos. Finalmente, los polímeros naturales no sólo son de origen proteico (colágeno, elastina, seda, etc.) sino también a base de carbohidratos (quitosano, ácido hialurónico, etc.) y han sido altamente modificados para mejorar su hidrofilia, solubilidad o adhesión celular a través del injerto de secuencias peptídicas como la RGD. En todos estos casos, se ha buscado la posibilidad de imprimir tejidos y órganos utilizando desde la bioimpresión aleatoria hasta biomanufactura aditiva.
Pese a todos estos avances, hoy en día no existe un material sintético adecuado para la sustitución de una arteria coronaria o venas/arterias de bajo calibre. Entonces, ¿qué ha cambiado? En palabras de Buddy Ratner (Universidad de Washington, E.U.A.), “los pacientes siguen muriendo hoy en día mientras que los expertos en biomateriales practican nanojuegos con una baja probabilidad de impacto futuro”. Esto obedece a que originalmente, la motivación de la investigación y el uso de los biomateriales estaba altamente dirigida hacia resolver las necesidades inmediatas de los pacientes y, siendo un poco más técnicos, el desarrollo de esta generación pasada de biomateriales estaba motivado por las demandas biomecánicas, el análisis de falla del implante o su fractura. Ahora, en el diseño de la nueva generación de biomateriales no sólo importa la composición del biomaterial o sus propiedades mecánicas, sino que se deben incluir componentes de nanotecnología, biología molecular y biología celular, es decir, incorporar y comprender a las biomoléculas y las proteínas de señalización en ellos y su interacción con el medio biológico. Además, se debe considerar que aunque se tenga esta motivación, la presión actual hacia los jóvenes se encuentra en una mayor productividad académica (artículos JCR, principalmente) y su transferencia hacia el sector productivo.
¿Y la relación con la industria, ’apá?
La actitud de las empresas del ramo es bastante intrigante. Por ejemplo, muchas empresas no apoyan proyectos relacionados con máquinas dializadoras porque son temas antiguos. Además, de acuerdo a Thomas Webster (Universidad de Northeastern, E.U.A.) el 70% de la industria no cree en los resultados de laboratorios académicos o clínicos, lo cual afecta severamente la investigación traslacional de la investigación en biomateriales. Sin embargo, cómo se explica que en Finlandia sigan creando empresas o nuevos productos relacionados con los biomateriales (Artic Biomaterials, Scaffdex) ahora que la Nokia ha dejado un gran vacío. El caso de la república de Irlanda merece especial atención, pues se ha convertido no sólo en un paraíso fiscal para empresas farmacéuticas, sino que también representa la puerta de entrada a Europa para muchas compañías norteamericanas.
Un reporte reciente sobre investigación traslacional de biomateriales en Europa sugiere que aunque los países tienden a especializarse, Química en Bélgica y España, Química y Biología en Alemania, Medicina en Rumania, Biomedicina en Italia, en Suiza se encuentra el portafolio más diversificado en disciplinas académicas4. Tal vez esto explique su gran impacto en el campo de los biomateriales.
En términos económicos, México ocupa el lugar 14 entre los países importadores de dispositivos médicos, que en el 2015 alcanzó la cifra de 3963 mdd5. En el mercado de dispositivos médicos, Italia es uno de los principales socios comerciales de México, exportando en el 2015, 16 mdd e importando, 55 mdd. En 2016, Johnson and Johnson ocupó el primer lugar (25.1 bdd) como la compañía más importante en México de dispositivos médicos, incluyendo productos para el tratamiento de la diabetes. Durante 2015, los estados de México con mayor presencia en el sector de los dispositivos médicos fueron Baja California (2428 mdd), Chihuahua (2250 mdd), Tamaulipas (1314 mdd), Sonora (399 mdd), Nuevo León (345 mdd) y la Ciudad de México (324 mdd). Sin embargo, al interior del país, existen bajos niveles de innovación.
Y ¿qué nos depara el futuro?
En el 2002, los grupos estaban más o menos separados y me atreví a decir, que en el norte de México se trabajaban más metales, en el centro del país más cerámicos, mientras que en el centro y el Sur, más polímeros y materiales compuestos. Esta distribución también ha cambiado: ahora nos vemos en la necesidad de incorporar materiales ajenos a nuestro conocimiento, con el fin de impartir propiedades multifuncionales. Esto hace difícil diferenciar o clasificar a los distintos grupos de investigación, pero lo que sí es evidente, es su continuo crecimiento. Recientemente, en el SLAP (Simposio Latinoamericano de Polímeros) 2016 y en el Macromex 2017, el número de contribuciones en el área de biomateriales de origen polimérico ha crecido notablemente. Tan notable es este crecimiento que se ha sugerido la posibilidad de organizar un congreso mexicano en Biomateriales e Ingeniería de Tejidos.
La investigación en biomateriales no sólo es importante en términos de divulgación, pero hay otras cuestiones que también son importantes de mencionar. Por ejemplo, vale la pena preguntarnos si los programas de estudios, ya sea de nivel licenciatura o de posgrado, son adecuados. ¿Qué es más importante, saber cuestiones básicas a profundidad que nos permitan adaptarnos a cualquier nuevo entorno, biológico por ejemplo, siendo un ingeniero de formación? ¿Es necesario dar todas estas herramientas multidisciplinarias desde la formación básica y crear programas más especializados? ¿Dónde podemos incluir tópicos de innovación, emprendedurismo o creación de empresas propias? ¿Dónde se aprende bioética o los pormenores de la experimentación animal?
¿Se puede concluir algo?
En mi opinión y a manera de conclusión, es evidente la necesidad de una mayor colaboración entre grupos. Para los que ya llevamos un tiempo en esto, lo mejor es apegarnos al antiguo sistema de zapatero a tus zapatos, ya que nos llevará mucho más tiempo aprender algo nuevo, dominarlo y ser experto en ello. No sólo esto, también será mucho más caro y es preferible usar la infraestructura de quien ya la tiene.
Para los jóvenes conservadores, sugiero proponer la creación de un centro nacional de materiales con aplicaciones médica con infraestructura para la caracterización fisicoquímica y mecánica de los materiales, cultivo celular y experimentación animal en un mismo sitio. En este centro, cada departamento o unidad estaría destinado a una aplicación. Para los jóvenes más arriesgados, propongo crear empresas en torno a aplicaciones poco invasivas, como los sustitutos dérmicos para úlceras o quemaduras, donde el mercado es de millones de dólares6. Además de este campo, los materiales dentales también son una buena alternativa, ya que el riesgo no es tan grande, pero respetando en todo momento, las sugerencias de los comités de bioética correspondientes. Para estos jóvenes emprendedores, una vez que la empresa funcione, la venden a una empresa mayor y, entonces, repiten el proceso de generación de una nueva empresa.
En mi opinión, los investigadores consolidados y los investigadores jóvenes deben resolver problemas nacionales, que también son problemas mundiales, como la diabetes, con herramientas de frontera. Esto es, utilizar continuamente los conocimientos recién generados en los distintos campos no sólo en el área biológica, sino también en la de materiales. Pese a que hoy en día podemos imprimir órganos y tejidos, no hay que ignorar que la biología también importa, es decir, podemos cambiar los métodos de fabricación para lograr lo que necesitamos. En términos de biocompatibilidad, tal vez sólo debamos preocuparnos de los macrófagos y su respuesta inflamatoria.
Referencias
- Williams, D.F. The Williams Dictionary of Biomaterials: Liverpool University Press; 1999.
- Williams, D.F. On the nature of biomaterials. Biomaterials. 2009;30(30):5897-909.
- Ratner, B. D. The Biocompatibility Manifesto: Biocompatibility for the Twenty-first Century. J. of Cardiovasc. Trans. Res. (2011) 4:523–527.
- A report on the Biomaterials Research Traslational in Europe. European Society for Biomaterials, 2017.
- Diagnóstico sectorial. Dispositivos Médicos. Estudio realizado por ProMéxico. Unidad de Inteligencia de Negocios, 2016.
- IBISWorld Industry Report OD4040. Cell Therapy in the US. January 2015. Dmitry Diment.
Sobre el autor:
El Dr. Cauich Rodríguez es Químico Industrial por la Facultad de Ingeniería Química de la Universidad Autónoma de Yucatán (1984-1988). Posteriormente realizó estudios de Maestría en la Universidad de Manchester (UMIST), Inglaterra, en Ciencia y Tecnología de Polímeros (1992-1994). El Dr. Cauich Rodríguez obtuvo el Doctorado en Queen Mary and Westfield College de la Universidad de Londres, Inglaterra (1994-1997). Desde 1998 es profesor-investigador del Centro de Investigación Científica de Yucatán, A.C. en la Unidad de Materiales, donde actualmente tiene la categoría de Investigador Titular D y realiza investigación en polímeros con aplicaciones médicas, incluyendo acrílicos para cementos óseos, poliuretanos para aplicaciones cardiovasculares y recientemente, modificación de materiales dentales. Como profesor ha impartido cursos sobre Síntesis de Polímeros, Biomateriales e Ingeniería de Tejidos. Ha realizado estancias sabáticas en el Instituto de Ciencia y Tecnología de Polímeros (ICTP-CSIC) en Madrid, España, y en la Universidad Técnica de Tampere, Finlandia. Es autor de más de 60 publicaciones indizadas en JCR, 10 capítulos de libros y ha dirigido tesis de Doctorado (13), Maestría (9) y Licenciatura (22). Actualmente es miembro del Sistema Nacional de Investigadores Nivel II.
Fuente: CICY




Pingback: Fuentes de Información – BioBell