Aclarando tu visión: cómo hacer transparentes los tejidos
Dr. Julio C. Chávez Zamora
Recientemente, se llevó a cabo el curso-taller sobre “Aclarado Óptico de Tejidos” en las instalaciones del Instituto de Biotecnología (IBt), en el área designada a la docencia de los Laboratorios de Investigación en Programas Institucionales (LINPI) . El curso fue organizado con la participación la Dra. Ana Cecilia Rivas, representante de Nikon de México; del Instituto Mexicano del Seguro Social (IMSS), y de las dos sedes del Laboratorio Nacional de Microscopía Avanzada (LNMA: en el Instituto de Biotecnología y en el Centro Médico Nacional Siglo XXI, cuyos responsables son el Dr. Christopher Wood y el Dr. Vadim Pérez Koldenkova, respectivamente). Los asistentes, provenientes de diferentes entidades académicas, tuvieron la oportunidad de procesar sus propias muestras (mediante la técnica Clarity, que explicaré más adelante); se procesaron embriones de peces, tejido oviductal (región que corresponde a las llamadas trompas de Falopio, del sistema reproductor femenino) y tejido cerebral de ratón, entre otros. El curso fue impartidó por el Dr. Michael Muntifering, integrante del Confocal Imaging Core, ubicado en el Cincinnati Children’s Hospital Medical Center en Ohio, EUA, quien es un experto en el tema.
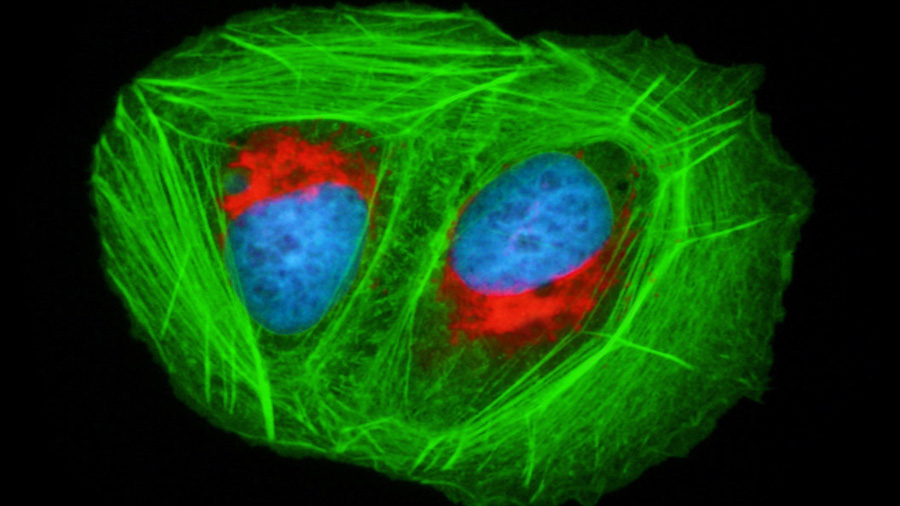
El “Aclarado Óptico de Tejidos” consiste en un conjunto de técnicas cuyo propósito es permitir la observación de la estructura tridimensional de diferentes tejidos, a profundidades de hasta 1 mm. Con estas técnicas, se puede observar el interior del tejido a profundidades que, sin este tratamiento, requeriría realizar cortes del mismo, lo cual aumenta el costo y el tiempo del procesamiento de las muestras. Otra ventaja de la técnica de aclarado es que es compatible con la presencia de proteínas fluorescentes: ya sea las producidas por el propio organismo (como la Proteína Verde Fluorescente o GFP, por sus siglas en inglés), por tinción durante el procedimiento (por ejemplo, con el colorante llamado Mitotracker, que tiñe las mitocondrias de las células), o bien, por el uso de anticuerpos acoplados a moléculas fluorescentes (por ejemplo, un anticuerpo unido a Alexa-Fluor) que reconocen su antígeno en las células del tejido.
Existen diferentes metodologías de aclarado, pero la finalidad de todas ellas es igualar el índice de refracción del tejido (que se define como el cociente de la velocidad de la luz en el vacío y la velocidad de la luz en el medio) con el medio de inmersión de la muestra. Es decir, hacer transparente el tejido, logrando una mayor penetración de la luz (ver foto 1). La transparencia de los tejidos se logra de diferentes maneras, aunque destacan los métodos basados en el uso de solventes orgánicos (con diferentes técnicas como las denominadas: Spalteholz clear, BABB y 3DISCO). Otra manera de lograrlo es mediante el uso de soluciones con un alto índice de refracción, como el uso de sustancias químicas con nombres como el 2,2′- tiodietanol (su nombre corto es TDE), o el FocusClear y la sacarosa (o azúcar de mesa, con la que se endulzan los alimentos). Una opción interesante, de la que les hablaré aquí, es la transformación del tejido mediante la técnica llamada Clarity. En esta técnica, se unen las proteínas y ácidos nucleicos del tejido a una malla o red de hidrogel (en este caso utilizamos el polímero de un compuesto llamado acrilamida) y después se eliminan los lípidos con un compuesto que tiene la función de un jabón o detergente.
En el protocolo de Clarity, normalmente se utiliza una sustancia química llamada foto-iniciador, cuya función es básicamente iniciar la formación del hidrogel. Por cuestiones técnicas, durante el curso empleamos un compuesto distinto, cuya función es catalizar la polimerización de los geles de acrilamida. Después de varias pruebas, se logró el objetivo de la formación del hidrogel y el posterior aclarado de los tejidos procesados.
El Dr. Muntifering además impartió un seminario en Oaxtepec, Morelos, como invitado del Congreso de Investigación del IMSS. En Oaxtepec, se profundizó en los aspectos teóricos de la adquisición y procesamiento de imágenes, además de compartir consejos prácticos y detalles técnicos acerca de los diferentes métodos de aclarado de tejidos.
Las muestras ya aclaradas o transparentadas, se observaron al microscopio en las instalaciones del LNMA (sede IBt), empleando los dos microscopios multifotónicos con los que cuenta el LNMA (ver foto 2).
Las imágenes obtenidas (foto 1) demostraron claramente a los participantes la utilidad de esta técnica, misma que podrán adoptar en sus estrategias experimentales.
Los especialistas interesados, pueden saber más acerca de las diferentes metodologías y aplicaciones del aclarado óptico de tejidos, en las siguientes publicaciones científicas:
- Tainaka K., Kuno A., Kubota S.I., Murakami T., Ueda H.R. (2016), Chemical Principles in Tissue Clearing and Staining Protocols for Whole-Body Cell Profiling. The Annual Review of Cell and Developmental Biology, 32:713–741.
- Silvestri L., Costantini I., Sacconi L., Pavone F.S. (2016), Clearing of fixed tissue: a review from a microscopist’s perspective. Journal of Biomedical Optics, 21(8), 081205.
El Dr. Julio César Chávez realiza su trabajo de Investigación en el laboratorio de la Dra. Claudia Treviño, como parte del Consorcio de Fisiología del espermatozoide, en el IBt.
Fuente: Revista Biotecnología en Movimiento



Pingback: Melanie Glastrong